Укажите сумму молярных масс (г/моль) алюминийсодержащих продуктов А и Б в следующей схеме превращений:
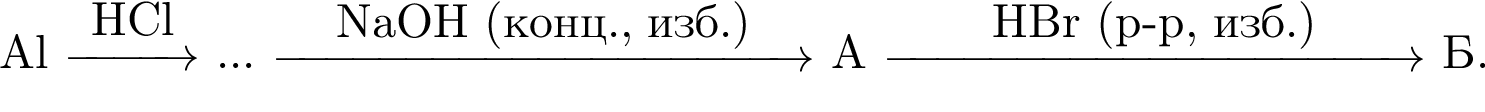
Укажите сумму молярных масс (г/моль) алюминийсодержащих продуктов А и Б в следующей схеме превращений:
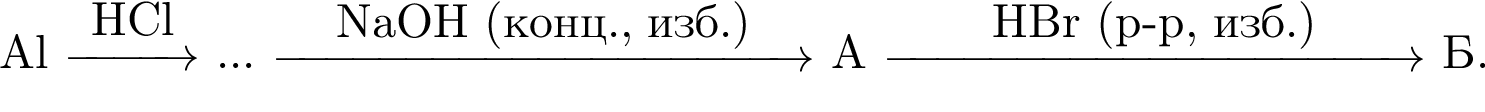
В порции вещества, формула которого ![]() содержится 1 моль атомов азота. Укажите объем (дм3) порции при н. у.:
содержится 1 моль атомов азота. Укажите объем (дм3) порции при н. у.:
Основные свойства высших оксидов предложенных элементов монотонно усиливаются в ряду:
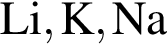
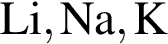
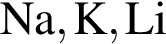
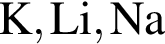
Правая часть сокращённого ионного уравнения имеет вид: _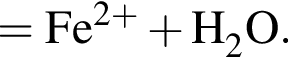 Уравнению соответствует реакция между:
Уравнению соответствует реакция между:
В четырёх пронумерованных пробирках находятся растворы неорганических веществ. О них известно следующее:
— вещества из пробирок 1 и 4 нейтрализуют друг друга;
— вещества из пробирок 3 и 1 реагируют между собой с образованием голубого осадка?;
— при добавлении к содержимому пробирки 2 вещества из пробирки 4 выпадает белый осадок.
Установите соответствие между названием неорганического вещества и номером пробирки, в которой находится раствор данного вещества.
А) хлорид бария
Б) нитрат меди(II)
В) гидроксид натрия
Г) серная кислота
1
2
3
4
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А2Б4В3Г1.
Гематит и сидерит являются природными соединениями:
Продуктом реакции присоединения является 2-метил-1,2-дихлорбутан. Исходное вещество имеет название:
С изменением степени окисления кремния протекают реакции:
а) 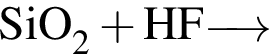
б) 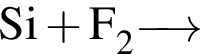
в) 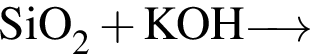
г) 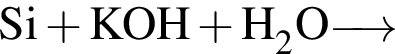
Масса соли, образовавшейся при взаимодействии алюминия с избытком концентрированного раствора гидроксида натрия, составила 594 г. Рассчитайте химическое количество (моль) электронов, перешедших от атомов алюминия к атомам водорода в результате реакции.
В отличие от разбавленной концентрированная серная кислота:
а) вытесняет ![]() из твёрдого
из твёрдого ![]() ;
;
б) НЕ реагирует с медью;
в) реагирует с  ;
;
г) при взаимодействии с цинком НЕ образует водород.
Кислотный оксид образуется при взаимодействии кислорода с веществом:
Основная соль может образоваться при взаимодействии азотной кислоты с каждым из гидроксидов, названия которых:
С помощью прибора, указанного на рисунке, способом вытеснения воды можно с минимальными потерями собрать газ:
В схеме превращений
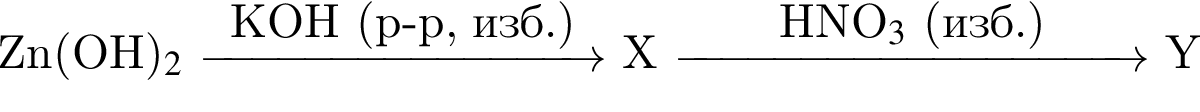
веществами ![]() и
и ![]() соответственно являются:
соответственно являются:
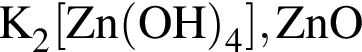
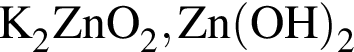
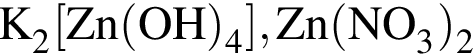
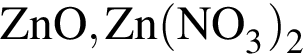
О протекании химических процессов в водном растворе свидетельствует:
Охарактеризуйте химическую связь в молекуле бромоводорода:
а) ковалентная полярная
б) ковалентная неполярная
в) одинарная
г) двойная
Одноатомными молекулами (н. у.) образовано простое вещество:
Степень окисления +2 имеют атомы серы в соединении: